|
Colaboración
con Datos Oficiales de Medicamentos
Base de datos del
INVIMA - Hoja de Cálculo de la CNPM
El equipo profesional que valida datos para su incorporación en la base
de datos del Sistema Integrado de Información de Medicamentos
del Vademécum Med-Informática y del Observatorio del Medicamento -
OBSERVAMED decidió reunir en esta página algunos ejemplos de errores
de digitación y demás inconsistencias que
encuentra en la base de datos del INVIMA y la hoja de cálculo
que reune los reportes a
la Comisión Nacional de Precios de Medicamentos, a fin de que los responsables del
mantenimiento de estas fuentes de información cuenten con un "recordatorio" que facilite
sus labores
de limpieza del sistema.
1.
Errores reportados en base de datos del INVIMA
1.1.
Modernización informática del INVIMA y errores de digitación
El Observatorio del Medicamento de la Federación Médica Colombiana ha
visto con agrado los esfuerzos de modernización informática del
Instituto Nacional de Vigilancia de Medicamentos y Alimentos INVIMA,
especialmente en lo relacionado con la reformulación de la base de datos
de registros sanitarios, la inclusión del Código ATC de los principios
activos y la generación del Código Unico del Medicamento CUM para todos
los productos y presentaciones disponibles en Colombia.
Lamentablemente, este
esfuerzo de modernización corre el riesgo de ser desvirtuado por
desafortunados errores de digitación e inconsistencias que son
inadmisibles en un organismo del más alto nivel científico y técnico
como es el INVIMA. Por esta razón, el Observatorio del Medicamento
publica en Internet, desde el año 2006, esta "página de
colaboración" que busca ayudar a los responsables de este tema a
detectar y corregir las inconsistensias que pueden restarle credibilidad y
utilidad a tan importante base de datos.
La siguiente tabla muestra
solo algunos ejemplos de
errores de digitación, detectados en una revisión preliminar de los 3
primeros grupos del
nuevo recurso de Codificaión ATC ofrecido por el INVIMA:
| Código ATC |
Observaciones: |
| A07E |
Error: No se pueden
consultar nivel X ATC |
| A07EC |
Antes decía ACIDO
AMINOSALICITICO
Debía decir: AMINOSALICILICO |
| B01AX |
Decía OTROS AGENTES
ANTILROMBATICOS Debe decir ANTITROMBOTICOS |
| B02 |
Decía ANTIHEMORRAC1COS
Debe decir ANTIHEMORRAGICOS |
| B02A |
Decía ANTIFRINOUTICOS
Debe decir ANTIFIBRINOLITICOS |
| B05ZA |
Decía HEMODIAIISIS
Debe decir HEMODIALISIS |
| B05ZB |
Decía HEMOFLLTRADOS
Debe decir HEMOFILTRADOS |
| C |
Error: No se pueden
consultar nivel X ATC |
| C01AB |
Decía GLUCOSIDOS DE
LA
ESTILA
Debía decir SCILLA |
| C01AX |
Decía OIROS GLUCOSIDOS
CARDIACOS Debía decir
OTROS |
| C01BA |
Decía ANTIARRITMICOS DE
CLASE
LA Debía decir 1A o 1a |
| C01BC |
Decía ANTIARRITMICOS DE
CLASE
LE Debía decir 1C o 1c |
| C01CA03 |
Decía
NOERPINEFRINA Debía decir NOREPINEFRINA |
| C01CA18 |
Decía
OCOTPAMINA Debía decir OCTOPAMINA |
| C01DA20 |
Decía NITRATOS ORG
NICOS Debía decir ORGANICOS |
| C10AC |
Decía DEIDOS BILIARES Debía decir ACIDOS BILIARES |
El Grupo C de SISTEMA CARDIOVASCULAR
actualmente está bloqueado. La versión inicial de esta tabla mostraba
los Códigos C01AB a C10AC con los errores de digitación que aquí se
mencionan. Al resolverse este bloqueo, ojalá todos estos errores
aparezcan corregidos
1.2. Inconsistencias
en Codificación ATC de Registros Sanitarios de medicamentos protegidos
por el Decreto 2085
El sitio web del INVIMA en su
sección de "consultas públicas" publica el seguimiento de los
medicamentos beneficiados por el Decreto 2085 del 2002(*) de protección
al uso de información no divulgada o "protección de datos de
prueba", que otorga protección de propiedad intelectual hasta por 5
años que pueden ser adicionales a los 20 años de la protección de la
patente. La página dedicada a este seguimiento puede verse en la dirección:
http://www.invima.gov.co/Invima///consultas/entidades_2085_protegidas.jsp?codigo=364
En la actualidad, dicha página muestra
hipervínculos a 3 informes que -con algunas diferencias de formato-
reportan las "entidades protegidas por el decreto 2085" a
septiembre 2008, enero 2008 y finales de 2007 más años anteriores. Este
grupo de medicamentos es particularmente importante porque reune las
novedades farmacológicas que ingresan al mercado colombiano y -con
frecuencia- son de "alto costo" y aparecen en los recobros al
FOSYGA incluso antes de ser medianamente conocidos en el mercado. Estos
productos, por ser los más recientemente ingresados a la base de datos
del INVIMA no deberían presentar las inconsistencias y errores de
digitación que mostramos a continuación.
(*) Para ver más sobre la importancia del Decreto 2085 visite la página
de seguimiento del Observatorio del Medicamento de la Federación Médica
Colombiana.
1.2.1. Informe de "entidades
protegidas" del mes de septiembre de 2008
El informe de moléculas protegidas por el Decreto 2085 correspondiente a
septiembre de 2008 puede verse en la dirección:
http://www.invima.gov.co/Invima///consultas/docs_entidades_2085/2008/entidadesprotegisayestudio_septiemb2008.htm
Este informe muestra 5 medicamentos
aprobados, de los cuales, dos productos de
DABIGATRAN (PRADAXA®
75 mg y de 110 mg de BOEHRINGER INGELHEIM), tienen registros sanitarios
con el Código ATC de CLOPIDOGREL:
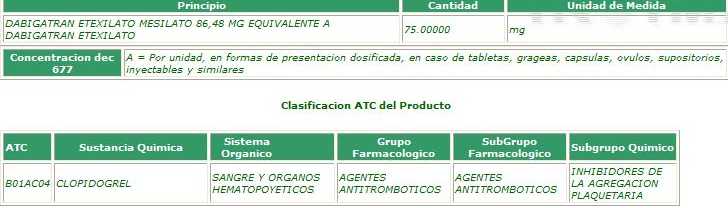
1.2.2. Informe de
"entidades protegidas" del mes de enero de 2008
El informe de moléculas protegidas por el Decreto 2085 correspondiente a
enero de 2008 puede verse en la dirección:
http://www.invima.gov.co/Invima///consultas/docs_entidades_2085/2008/RETAPAMULINA.htm
Este informe incluye dos medicamentos, VILDAGLIPTINA
(GALVUS®
de NOVARTIS) cuyo registro sanitario muestra el Código ATC de REPAGLINIDA
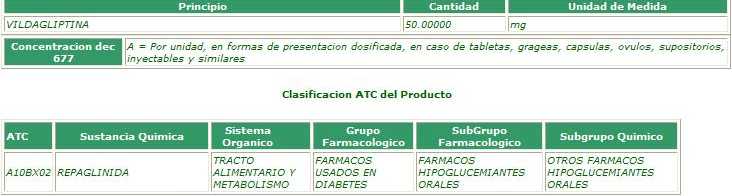
Y ROTIGOTINA
( NEUPRO® de BIOPAS) cuyo registro sanitario muestra el Código ATC de
LEVODOPA.
Adicionalmente,
el informe dice NEUPRO en columna principios activos y ROTIGOTINA en
columna marcas. Hay traslocación
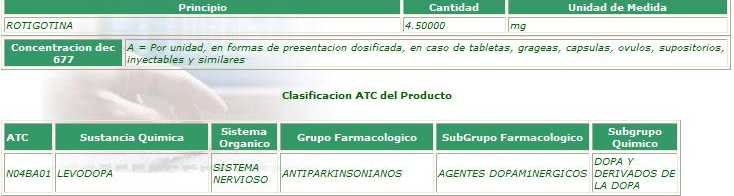
En
este informe también se encuentra LAROPIPRANT (CORDAPTIVE de MERCK SHARP
& DOHME) que en el Acta INVIMA No. 5 de 2008 aparece como
HIPOGLICEMIANTE en lugar de HIPOLIPEMIANTE. Ver Acta:
http://www.invima.gov.co/Invima/consultas/docs_actas/medicamentos/2008/acta5_2008_medicamentos.pdf
1.2.3. Informe de
"entidades protegidas" del año 2007 y anteriores
El informe de entidades protegidas por Decreto 2085 del 2007 y anteriores
puede verse en la dirección:
http://www.invima.gov.co/Invima///consultas/docs_entidades_2085/2007/cuadro%20virtual%20entidades%20protegidas%20oct2007.htm
Este informe muestra otros 3 medicamentos cuyo Código
ATC en el registro sanitario está errado:
ABATACEPT (ORENCIA® de BRISTOL-MYERS SQUIBB) cuyo registro sanitario
muestra Código ATC de IBUPROFENO

y DASATINIB (SPRYCEL® 50
mg y 70 mg de BRISTOL-MYERS SQUIBB) cuyos registros sanitarios
aparecen con el Código ATC de IODOXAMICO ACIDO
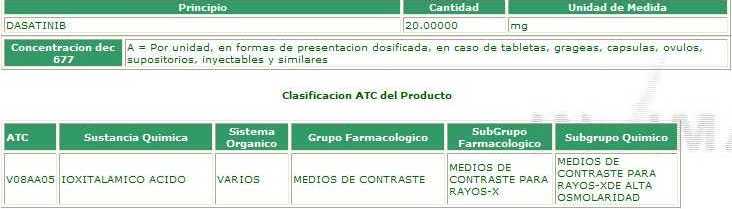
Finalmente,
en este informe pueden verse además los siguientes errores de digitación:
Dice TECNETEPLASA y debe decir TENECTEPLASA.
Dice DERIFENACINA y debe decir DARIFENACINA
Dice ALEMTUZAMAB y debe decir ALEMTUZUMAB
Dice PREGAPTANIB y debe decir PEGAPTANIB
Dice IBRITUMOCAB TIUXETAN y debe decir IBRITUMOMAB
TIUXETAN
Dice DEFERAXIROX y debe decir DEFERASIROX
http://www.invima.gov.co/Invima///consultas/docs_entidades_2085/2007/cuadro%20virtual%20entidades%20protegidas%20oct2007.htm
1.2.4. Importancia de los
errores de Codificación ATC en los registros sanitarios de medicamentos
protegidos por el Decreto 2085
Ninguno de los medicamentos mencionados lineas arriba está incluido en el
Plan Obligatorio de Salud (POS), pero prácticamente todos impactan en
mayor o menor medida las cuentas de los prestadores y administradores de
servicios de salud y finalmente los recobros al FOSYGA. Es aquí donde la
codificación ATC de estos productos puede cobrar significancia y pasar a
tener un impacto económico. Y la explicación sería la siguiente:
Cuando estos medicamentos no
incluidos en el POS deben ser recobrados al FOSYGA, la entidad que recobra
debe relacionarlos con un "homólogo" en el POS. Para este
efecto, el Ministerio de la Protección Social publicó hace varios años
un listado de "homólogos" que lamentablemente nunca pudo ser
perfeccionado. Por esta razón, en la práctica, se está imponiendo el
uso de la codificación ATC. En esta situación, lo lógico sería que
todos nos basáramos en el Código ATC asignado por el INVIMA, pero, ¿cómo
hacerlo, si la base de datos del INVIMA presenta este tipo de
inconsistencias?.
1.3.
Algunos ejemplos de error de digitación en Registros Sanitarios
Estos son algunos ejemplos tomados al azar en revisión del 9 de enero de
2007 y que persisten en la base a 31 de octubre de 2007, cuando -se supone-
ya culminó la fase de validación de la
Circular DG 100-00420-06:
| Fecha |
Registro |
Dice |
Debe decir |
| 09ene07 |
INVIMA M-012417 |
DILTRAZEM |
DILTIAZEM? |
| 09ene07 |
INVIMA 2004M-0003767 |
ULCERA
PAPTICA |
PEPTICA? |
| 09ene07 |
INVIMA 2003M-0002853 |
IPATROPIO |
IPRATROPIO? |
| 09ene07 |
INVIMA 2003M-0002804 |
DUOASTALIN |
Laboratorio reporta DUASTALIN |
| 09ene07 |
INVIMA 2005M-0004089 |
CIPLATROPIUN |
CIPLATROPIUM? |
| 09ene07 |
INVIMA 2005M-0004454 |
LAMIRACOXIB |
LUMIRACOXIB? |
| 09ene07 |
INVIMA 2003M-0002999 |
DOLIVUM |
Laboratorio reporta
DOLIVIUM |
| 09ene07 |
INVIMA 2002
M-004811-R2 |
ACEITE
DE RICINO OFICIAL |
OFICINAL? |
| 09ene07 |
INVIMA M-012122 |
DURNATE,
INTERVANCIONES, COMPONENETES |
DURANTE,
INTERVENCIONES, COMPONENTES? |
|
2.
Observaciones
a Hoja de cálculo de la Comisión Nacional de Precios de
Medicamentos - CD Reportes de Laboratorios a finales de 2006
Recomendaciones
GENERALES:
Revisado del CD que
periódicamente nos envía la Secretaría Técnica de la Comisión
Nacional de Precios de Medicamentos
insistimos en algunas de las
recomendaciones que publicamos en el Boletín Informática
& Salud
- Obligación
de Reportar:
Pese a la existencia de antecedentes como la Circular No. 6 de
2002 que pasó 28 laboratorios del régimen de "Libertad
Vigilada" a "Libertad Regulada" por no informar
oportunamente sus precios a la CNPM, algunos laboratorios como
Best, Colphar, Colpharma, Delta, Dermacare, etc. no
presentan reportes o llevan más de un año sin reportar.
- Grupo en
que Clasifica:
Un gran número de productos que reportan régimen de
"Libertad", "Libertad Total", etc.
técnicamente deben pasar a una de las 3 opciones correctas:
"Libertad Vigilada", "Libertad Regulada" y
"Control Directo"
- Registro
Sanitario:
De 13.394 productos registrados en el CD,
aproximadamente 3.200 tiene registros sanitarios correctos, es
decir, iguales a los que aparecen en la base de datos del
INVIMA y en los empaques de los productos. Los restantes (más
de 10.000.-) presentan algún tipo de error que los hace
diferentes y generan confusión.
Recordemos que los Registros
Sanitarios de la época en que los otorgaba el Ministerio de
Salud comienzan con la letra M. Ejemplo: M-008197
VOLTAREN 25 MG GRAGEAS de CIBA GEIGY AG. (NOVARTIS)
Los primeros Registros otorgados por el INVIMA tienen su
nombre, la letra M de Medicamento y la Renovación cuando
existe. Ejemplo: INVIMA M-012174-R1 ARTREN CAPSULAS de
MERCK S.A.
Los Registros posteriores otorgados por el INVIMA tienen además
el año. Ejemplo:
INVIMA 2006M-003927 R1 INFLANAX de PROCAPS S.A.
Es de capital importancia señalar que NINGUNO de los
elementos del Registro Sanitario puede ser mutilado o alterado
porque inmediatamente genera falsedad, origina duplicados y
otros errores en procesos que exigen este dato como las
licitaciones, los recobros, etc.
- Nombre
Comercial del Producto:
Aunque legalmente el nombre que debería reportarse es
el que aparece en el Registro Sanitario, varias firmas farmacéuticas
emplean formatos arbitrarios, observándose casos con menos
datos que el registro y casos de nombres hasta con presentación.
Recomendamos utilizar el nombre, la concentración y -cuando
se justifique- la forma farmacéutica.
- Nombre Genérico
del Producto:
Este campo corresponde a la denominación genérica, científica
o común internacional (DCI) y en los primeros formatos se
llamó "Composición". Por alguna razón, varios
laboratorios siguen reportando aquí -erróneamente- las
"indicaciones" del producto. Mientras se define
mejor la parametrización de este campo, sugerimos respetar la
nomenclatura internacional.
- Forma
Farmacéutica:
Este campo está correcto en cerca del 70% de los casos.
Para los casos de error, es necesario parametrizar mejor las
opciones en la norma. Mientras esto sucede, sugerimos respetar
las formas farmacéuticas que aparecen en las registros
sanitarios.
- Concentración:
Algunos Laboratorios reportan este campo la
"composición" es decir el nombre del principio
activo, generando repeticiones innecesarias y contrarias a la
norma. Sugerimos respetar las indicaciones de las circulares
de la CNPM.
- Presentación
Comercial:
Algunos Laboratorios
reportan presentaciones extensas con detalles innecesarios y
otros con datos insuficientes. Como en el anterior punto,
sugerimos respetar las indicaciones de las circulares de la
CNPM.
-
Precios:
La norma dice que debe reportarse el Precio Promedio a
Distribuidor "entendiéndose como tal el resultante
del promedio aritmético obtenido de los promedios de precios
de los cuatro canales de comercialización establecidos a
saber: mayoristas y cooperativas; cajas de compensación;
almacenes de cadena y grandes superficies; droguerías
detallistas" (No se menciona el canal Institucional) y el
Precio Sugerido al Público "para los medicamentos
sometidos al régimen de Libertad (vigilada o regulada) de
precios, es el Precio Sugerido al Público y para los
medicamentos sometidos a Control Directo de Precios es el
Precio Máximo de Venta al Público"
En algunos laboratorios se observa traslocación de estos
precios y en otros falta de datos o error en relación con el
régimen que aplica.
Algunas
OBSERVACIONES ESPECIFICAS:
- AH ROBBINS
Errores de formato en "Registros Sanitarios",
"Indicaciones" en "Nombre Genérico",
"Nombres Genéricos" en "Concentración"
y reportes solo hasta 3er. trimestre 2005.
- ABBOTT
Algunos errores de formato en "Registros Sanitarios" y en
"Nombre Genérico". En reportes del 2do. trimestre
de 2006 se insertaron celdas en lugar de líneas para
incluir 3 nuevos produtos y se alteró el ordenamiento de
precios de los demás productos. Por fortuna, este error
afectó solamente los datos de este laboratorio.
- ACTIFARMA
"Nombres Genéricos" con
"Concentraciones" y "Concentraciones"
con "Presentación"
- AKZO NOBEL - ORGANON
"Concentraciones" extensas con "Nombre
Genérico"
- ALCON
Errores de formato en "Registros Sanitarios" y
"Grupo"
- ALGUVER
Errores de formato en "Registros Sanitarios",
"Indicaciones" en "Nombre Genérico",
"Nombres Genéricos" en "Concentración"
y reportes solo hasta 3er. trimestre 2005.
- ALLERGAN
Errores de formato en "Registros Sanitarios" y
"Grupo"
- ALLIANCE
"Concentraciones" con "Nombres
Genéricos"
- AMAREY NOVA MEDICAL
Errores de formato en "Registros Sanitarios"
- AMERICA
Algunas "Concentraciones" con "Nombres
Genéricos"
- El Registro M-01438-R1 reportado para CEFALEXINA 500 mg está traslocado. El Registro correcto es INVIMA M- 010438-R1 y corresponde a LEXBAC 500 mg de AMERICA
- AMERICAN GENERICS
- El Registro M-013867 reportado para ALBENDAZOL 100 mg / 5 mL (2%) corresponde a FAMIDOX 100 mg / 5 mL de PAULY
- El Registro M-009580 reportado para ALBENDAZOL 200 mg corresponde a FAMIDOX 200 mg de PAULY
- El Registro M-012840 reportado para CARBONATO DE CALCIO 600 mg de AMERICAN_GENERICS corresponde a CALDORAL 600 mg de PAULY
- El Registro M-003546 reportado para FUROSEMIDA 40 mg está errado. El correcto es INVIMA 2005 M-003543 R1
- ANGLOPHARMA
El reporte del 2do. trimestre 2006 muestra 19 introducciones
de productos y presentaciones, 15 de las cuales no tienen
Registro Sanitario (¿error del laboratorio o de la
transcripción?); Diclofenaco 50 mg grageas dice x 250
ampollas en presentación; Dinitrato de Isosorbide no trae
dato de presentación; Hidrocortisona de 25 mg en tabletas
no existe y el registro reportado corresponde a la crema;
Hidroxicina 25 mg x 250 tabletas tiene RS del jarabe y no
tiene el dato de PPD; Loratadina 10 mg tiene el RS vencido y
precio sugerido al público de 444.425 cuando el promedio a
distribuidor es solo de Col$ 10.000.-; Metformina 850 mg
tiene error en presentación hospitalaria (no puede ser de
20 tabletas y valer 4 veces más que la presentación de 30
tabletas); Propranolol 40 mg nueva presentación
hospitalaria no tiene dato de presentación y su RS
corresponde a 80 mg y está vencido; Sildenafil 50 mg nueva
presentación por 4 tabletas muestra precios 5 veces inferior a nueva
presentación por 1 tableta y más de 10 veces inferior a
antigua presentación por 2 tabletas.
- APOTECARIUM (ANZG LTDA)
La búsqueda - UMEZAR - no produjo ningún resultado en la base de datos del INVIMA. EL REGISTRO SANITARIO INVIMA 2004M-0003701 CORRESPONDE A ZEMTIA®
El reporte del 2do. trimestre 2006 muestra 3 introducciones,
ninguna de las cuales tiene Registro sanitario ni
Presentación. Esto último impide el cálculo de precios
uni-dosis e interfiere con los análisis por este concepto.
14 de los 41 productos de esta línea no tienen dato de
Nombre genérico o Principio activo.
- BAXTER
Errores de formato en "Grupo en que clasifica",
"Nombres Genéricos" en
"Concentración" y reportes solo hasta 3er. trimestre 2005.
- BEST
- El Registro M-012205 reportado para AMBROXOL 30 mg / 5 mL de BEST está errado. El correcto es INVIMA M-012505 de BEST
- BIOGEN
- El Registro M-009672-R1 reportado para ACICLOVIR 250 mg de BIOGEN corresponde a VIREX 250 mg de BIOGEN
- El Registro M-006693 reportado para BECLOMETASONA DIPROPIANATO 50 mcg de BIOGEN corresponde a BRONCONOX 50 mcg de ALDO_UNION
- El Registro INVIMA M-005468 reportado para BECLOMETASONA DIPROPIANATO 250 mcg de BIOGEN corresponde a BRONCONOX 250 mcg de ALDO_UNION
- El Registro M-013232 reportado para FLUCONAZOL 200 mg de BIOGEN corresponde a NOBZOL 200 mg de BIOGEN
- BIOGENERICOS
- El Registro sanitario M-012041 reportado para SECNIDAZOL 750 mg corresponde a ALBENDAZOL 200 MG SUSPÈNSION INVIMA M-012041 de BIOGENERICOS. El Registro correcto es INVIMA M-0012430
- BIOTOSCANA
El reporte del 2do. trimestre 2006 muestra 14 introducciones
de las cuales 12 no tienen dato de Laboratorio, Régimen que
aplica ni Registro sanitario. 2 Tuberculinas sin Registro
sanitario, de las cuales la última aparece con la misma
presentación por 2 dosis, pero con precios casi 4 veces
superiores.
- BUSSIE
- El Registro M-000831 reportado para ALBENDAZOL 100 mg / 5 mL corresponde a BENEXIN 100 mg / 5 mL de BUSSIE
- El Registro M-011404 reportado para CARBAMAZEPINA 100 mg / 5 mL de BUSSIE corresponde a SIGILEX 100 mg / 5 mL de BUSSIE
- El Registro M-006692 reportado para CARBAMAZEPINA 200 mg de BUSSIE corresponde a SIGILEX 200 mg de BUSSIE
- El Registro M-011179-R1 reportado para CIPROFLOXACINA 250 mg de BUSSIE corresponde a CIGRAM 250 mg de BUSSIE
- El Registro M-011296-R1 reportado para CIPROFLOXACINA 500 mg de BUSSIE corresponde a CIGRAM 500 mg de BUSSIE
- El Registro M-001002 reportado para PROPRANOLOL 40 mg corresponde a STABLIX 40 mg de BUSSIE
- El Registro M-001739 reportado para PROPRANOLOL 80 mg corresponde a STABLIX 80 mg de BUSSIE
- El Registro M-003991 reportado para TRIMETOPRIM+SULFAMETOXAZOL 160 mg / 800 mg corresponde a SULFAPRIM F 160 mg / 800 mg de BUSSIE
- CARIBE
- El Registro M-010429-R1 reportado para ACETAMINOFEN 100 mg / mL de CARIBE corresponde a KENOX 100 mg / mL de CARIBE
- El Registro M-010484-R1 reportado para ACETAMINOFEN 150 mg / 5 mL de CARIBE corresponde a KENOX 150 mg / 5 mL de CARIBE
- CHALVER
- El Registro M-012182 reportado para OMEPRAX 40 mg coresponde a BETARRETIN.
La búsqueda de OMEPRAX en la base de datos del INVIMA solo encuentra OMEPRAX CÁPSULAS 20 MG (No aparece la concentración de 40 mg)
- COLMED
- El Registro M- 003671 reportado para ERITROMICINA 250 mg / 5 mL de COLMED corresponde a ERIBLAN 250 mg / 5 mL de COLMED pero reportado por PROCAPS
- COLPHAR
- El Registro M-001529 reportado para ALBENDAZOL 200 mg corresponde
a NEMACIST 200 mg de COLPHAR que está vencido
- COLPHARMA
Este Laboratorio está activo pero no aparecen sus datos de
disponibilidad y precios en el CD de la CNPM
- DIZMOFAR
-
La búsqueda - 03012 - del Registro
M-003012 reportado para CAPTOPRIL 50 mg no produjo ningún resultado en la base de datos del
INVIMA. La búsqueda de "CAPTOPRIL" enlistó 134 registros
de los cuales solo INVIMA M-001580 corresponde a CAPTOPRIL
25 mg de LABORATORIOS DIZMOFAR y está vencido.
- El registro M-008881-R1 reportado para AMPICILINA 500 mg de DIZMOFAR está errado. La búsqueda de AMPICILINA produce 193 registros de los cuales solo 1 (AMPICILINA 1g) corresponde a DIZMOFAR.
- ESSEX
- El Registro INVIMA M-002959 reportado para ALATRIN D JARABE corresponde a ALATRIN SIMPLE de ESSEX FARMACEUTICA S.A. y está vencido. El Registro M-002956 que aparece en la descripción no se encuentra en la base de datos del INVIMA, donde tampoco aparece ningún registro para ALATRIN D JARABE
- GENERICOS DE COLOMBIA
- El Registro M-012236/01 reportado para ACICLOVIR 200 mg de GENERICOS_COLOMBIA corresponde a VIRCIDAL 200 mg de CHALVER
- El Registro M-011839/00 reportado para ACICLOVIR 250 mg de GENERICOS_COLOMBIA corresponde a VIRCIDAL 250 mg CHALVER
- El Registro M-009753-R1 reportado para ALBENDAZOL 100 mg / 5 mL corresponde a ROTOPAR 100 mg / 5 mL de CHALVER
- El Registro M-009752-R1 09 reportado para ALBENDAZOL 200 mg corresponde a ROTOPAR 200 mg de CHALVER
- El Registro INVIMA M-004946 reportdo para CEFTRIAXONA 500 mg de GENERICOS_COLOMBIA corresponde a CEFTRIAN 500 mg de CHALVER
- El Registro M-012148/00 reportado para CIPROFLOXACINA 100 mg / 10 mL de GENERICOS_COLOMBIA corresponde a QUINOPRON 100 mg / 10 mL de CHALVER
- El Registro M-012033/00 reportado para CIPROFLOXACINA 250 mg de GENERICOS_COLOMBIA corresponde a QUINOPRON 250 mg de CHALVER
- El Registro M-011840/00 reportado para CIPROFLOXACINA 500 mg de GENERICOS_COLOMBIA corresponde a QUINOPRON 500 mg de CHALVER
- El Registro M-006478-R1/04 reportado para CLOTRIMAZOL 1% de GENERICOS_COLOMBIA corresponde a INVIMA 2003M-006478-R2 de CUTAMYCON 1% CHALVER
- El Registro M-006656-R1/03 reportado para CLOTRIMAZOL 100 mg de GENERICOS_COLOMBIA corresponde a CUTAMYCON 100 mg de CHALVER
- El Registro M-009757-R1/07 reportado para DICLOXACILINA 500 mg de GENERICOS_COLOMBIA corresponde a DIXALIN 500 mg de CHALVER
- El Registro M-012249 reportado para FLUOXETINA 20 mg de GENERICOS_COLOMBIA corresponde a DEPREXIN 20 mg de CHALVER
- El Registro sanitario M-012231 reportado para LORATADINA 10 mg corresponde a HISTALORAN de CHALVER
- El Registro M-012627 reportado para LORATADINA 5 mg / 5mL corresponde a HISTALORAN 5 mg / 5 mL de CHALVER
- El Registro M-012239 reportado para OMEPRAZOL 20 mg corresponde a PRAZOGAS 20 mg de CHALVER
- El Registro M-006654-R1 reportado para RANITIDINA 150 mg de GENERICOS_COLOMBIA corresponde a RANIOGAS 150 mg de CHALVER
- El Registro M-13607/09 reportado para RANITIDINA 300 mg de GENERICOS_COLOMBIA corresponde a RANIOGAS 300 mg de CHALVER
- El Registro M-006418-R1/04 reportado para RANITIDINA 50 mg / 2 mL de GENERICOS_COLOMBIA corresponde al INVIMA 2004 M-006418-R2 de RANIOGAS 50 mg / 2 mL de CHALVER
- LABINCO
- El Registro 2003M-00022244 reportado para ACETAMINOFEN 150 mg / 5 mL de LABINCO está errado. El correcto es INVIMA 2003M-0002224
- LA_SANTE
- Registro INVIMA 2002M-0001559 Reportado para COMPLEJO B corresponde a PAX JARABE PARA LA TOS 5%.
- ESOZ 20 mg y ESOZ 40 mg tienen los registros sanitarios
invertidos
- Registro INVIMA 2004M-0003451 reportado como SULFACETAMINA
es SULFACETAMIDA
- LAPROFF
- El Registro M-011682 reportado para CETIRIZINA 10 mg de LAPROFF corresponde a CETILER 10 mg de LAPROFF
- LETI
- El Registro M-004892 reportado para ACICLOVIR 200 mg de LETI no se encuentra en la base de datos del INVIMA. La búsqueda de "ACICLOVIR" enlistó 79 registros de los cuales ninguno corresponde a LETI
- La búsqueda - 06941 - del Registro M-006941 reportado para CAPTOPRIL 50 mg no produjo ningún resultado en la base de datos del INVIMA.
La búsqueda de "CAPTOPRIL" enlistó
134 registros de los cuales ninguno corresponde a LABORATORIOS LETI DE COLOMBIA
S.A.
- MEMPHIS
- El Registro M-014989 reportado para AMIKACINA 100 mg / 2 mL de MEMPHIS está errado. El correcto es INVIMA 2006M-0006466
- MERCK
- El Registro M-000678 reportado para METFORMINA 850 mg de MERCK corresponde a INVIMA 2005 M-000678 R1 de GLUCOPHAGE 850 mg de MERCK
- NAKUCH
Reporta DIPERIN, EXTORGEN y UR-SET con nombre y registro sanitario que no aparecen en la
Base de Datos del Invima
- NOBEL
- El Registro M-010554-R1 reportado para RANITIDINA 150 mg coresponde a SAMPEP 150 mg de NOBEL
- ORGANON
Registro INVIMA 2003M-0002719 ONCOTICE Caja x 1 Vial PSP
617.900.- y Caja x 3 Viales PSP 350.000.-??
- OPHALAC
- La búsqueda - 12922 - del Registro Sanitario M-012922 reportado para PROPAFENONA 150 mg no produjo ningún resultado en la base de datos del INVIMA. La búsqueda de PROPAFENONA no produjo ningún resultado de OPHALAC
- El Registro 2002M-0001112 reportado para CARBONATO DE CALCIO 600 mg de OPHALAC corresponde a CALTROX 600 mg de OPHALAC
- El Registro M-14350 reportado para CEFRADINA 500 mg de OPHALAC está errado. El correcto es INVIMA 2004M-0003680
- PAULY
Reporta "INFUSID NP" Registro Sanitario M-014646. El
Registro Sanitario INVIMA 2003 M-014646-R1 corresponde a "ACIDO FUSIDICO"
de AMERICAN_GENERICS del mismo conglomerado. "INFUSID NP" No
aparece en la base de datos del INVIMA
- PHARMARKETING-LAB_CHILE
- La búsqueda - 010949 - del Registro M-010949 reportado para
ACETAMINOFEN 100 mg / mL no produjo ningún resultado en
la base de datos del INVIMA
- La búsqueda - 010948 - del Registro M-010948 reportado para
ACETAMINOFEN 500 mg no produjo ningún resultado en
la base de datos del INVIMA
- El Registro M-012458 reportado para ACIDO ACETIL SALICILICO 500 mg de LAB_CHILE no aparece en la base de datos del INVIMA. La búsqueda de ACIDO ACETIL SALICILICO enlistó 33 registros de los cuales ninguno corresponde a PHARMARKETING-LAB_CHILE
- El Registro Sanitario M-010866 Reportado por ALBENDAZOL 200 mg Corresponde a GARHOCAINA INVIMA M- 010866- R1 de LABORATORIOS FARPAG LTDA
(4 presentaciones)
- El Registro Sanitario M-010867 Reportado por ALBENDAZOL Corresponde a RODIX TABLETAS INVIMA M-010867-R1 de GALENO QUIMICA S.A.
(12 presentaciones)
- El Registro M-010868 reportado para ALPRAZOLAM 0,25 mg de PHARMARKETING-LAB_CHILE no se encuentra en la base de datos del INVIMA. La búsqueda por ALPRAZOLAM no produce ningún producto cuyo laboratorio sea PHARMARKETING-LAB_CHILE (5 presentaciones)
- El Registro M-011135 reportado para ALPRAZOLAM 0,5 mg de PHARMARKETING-LAB_CHILE no se encuentra en la base de datos del INVIMA. La búsqueda por ALPRAZOLAM no produce ningún producto cuyo laboratorio sea PHARMARKETING-LAB_CHILE (5 presentaciones)
- Registro Sanitario M-011091 Reportado por AMBROXOL Corresponde
a 32697 DRISTANCITO- AF
- Registro Sanitario M-012466 Reportado por AMBROXOL Corresponde
a 38975 DRUGPANIL M-012466 Vencido
- Registro Sanitario M-011147 de AMOXICILINA 250 mg corresponde a
34554 CLIFAR Vencido 1999/09/07
- La búsqueda - 12350 - del Registro Sanitario M-012350
reportado para AMOXICILINA no produjo ningún resultado en
la base de datos del INVIMA
- La búsqueda - 10944 - del Registro M-010944 reportado para BROMAZEPAM 3 mg no produjo ningún resultado en la base de datos del INVIMA
(2 presentaciones)
- La búsqueda - 010789 - del Registro M-010789 reportado para CARBONATO DE CALCIO 500 mg no produjo ningún resultado en la base de datos del INVIMA
- El Registro M-007509 reportado para CEFOTAXIMA 1 g de PHARMARKETING-LAB_CHILE no se encuentra en la base de datos del INVIMA. La búsqueda por CEFOTAXIMA no produce ningún producto cuyo laboratorio sea PHARMARKETING-LAB_CHILE (2 presentaciones)
- Los Registros M-010538 y M-007507 reportados para CEFRADINA 500 mg de PHARMARKETING-LAB_CHILE no se encuentra en la base de datos del INVIMA. La búsqueda por CEFRADINA no produce ningún producto cuyo laboratorio sea PHARMARKETING-LAB_CHILE (2 presentaciones)
- El Registro M-011145 reportado para CIPROFLOXACINA 250 mg de PHARMARKETING-LAB_CHILE no se encuentra en la base de datos del INVIMA. La búsqueda por CIPROFLOXACIN no produce ningún producto cuyo laboratorio sea PHARMARKETING-LAB_CHILE (6 presentaciones)
- El Registro M-010980 reportado para CLORAMFENICOL 0.5 %
corresponde a TRIMEBUTINA INVIMA M-010980-R1 de LABORATORIOS
SYNTHESIS LTDA. Y CIA. S.C.A. (6 presentaciones)
- El Registro M-011036 reportado para CLORANFENICOL 250 mg
corresponde a ACEITE DE HIGADO DE TIBURON CAPSULA BLANDA INVIMA
M-011036-R1 de INVERSIONES VASCO LTDA. (5 presentaciones)
- La búsqueda búsqueda - 10816 - del Registro sanitario
M-010816 reportado para CLORDIAZEPOXIDO 10 mg no produjo ningún
resultado enla base de datos del INVIMA oias/nov06 (3
presentaciones)
- El Registro M-010627 reportado para CLOTRIMAZOL 1% de PHARMARKETING-LAB_CHILE corresponde a RANITER TABLETAS INVIMA M-010627-R1. La búsqueda de CLOTRIMAZOL en la base de datos del INVIMA muestra 127 registros de los cuales ninguno pertenece a PHARMARKETING-LAB_CHILE
- La búsqueda - 06993 - del Registro M-006993 reportado para DICLOFENACO 25 mg no produjo ningún resultado en la base de datos del INVIMA
(6 presentaciones)
- La búsqueda - 07499 - del Registro M-007499 reportado para DICLOFENACO 50 mg no produjo ningún resultado en la base de datos del
INVIMA (2 presentaciones).
- La búsqueda - 010811 - del Registro M-010811 reportado para DICLOFENACO 75 mg / 3 mL no produjo ningún resultado en la base de datos del
INVIMA (5 presentaciones).
- La búsqueda - 011604 - del Registro M-011604 reportado para DICLOFENACO DIETILAMONIO Crema al 1, 2 y 3 % no produjo ningún resultado en la base de datos del INVIMA. Las 3 concentraciones se reportan con el mismo Registro sanitario, cuando habitualmente el INVIMA asigna un registro a cada concentración.
- La búsqueda de "DICLOFENAC" enlistó 164 registros de los cuales ninguno pertenece a PHARMARKETING o LABORATORIOS CHILE
- La búsqueda - 011038 - del Registro M-011038 reportado para
ENALAPRIL 5 mg no produjo ningún resultado en la base de datos del
INVIMA (9 presentaciones).
- La búsqueda - 10707 - del Registro M-010707 reportado para GEMFIBROZIL 300 mg de PHARMARKETING-LAB_CHILE no produjo ningún resultado en la base de datos del
INVIMA (6 presentaciones) (6 presentaciones). La búsqueda GEMFIBROZIL produce un listado de 50 productos ninguno de los cuales corresponde a PHARMARKETING-LAB_CHILE.
- La búsqueda - 10432 - del Registro M-010432 reportado para GEMFIBROZIL 900 mg de PHARMARKETING-LAB_CHILE no produjo ningún resultado en la base de datos del INVIMA (6 presentaciones). La búsqueda GEMFIBROZIL produce un listado de 50 productos ninguno de los cuales corresponde a PHARMARKETING-LAB_CHILE.
- La búsqueda - 010436 - del Registro M-010436 reportado para LORATADINA 5 mg / 5mL no produjo ningún resultado en la base de datos del INVIMA (9 presentaciones).
- El Registro M-011139 reportado para PREDNISONA 5 mg corresponde
a RETIN A CREMA DE 0,025% INVIMA M-011139-R1 de JANSSEN CILAG S.A.
(2 presentaciones)
- La búsqueda - 011141 - del Registro M-011141 reportado para PROPRANOLOL 40 mg no produjo ningún resultado en la base de datos del INVIMA (5 presentaciones).
- El Registro M-007498 reportado para 7 de 9 presentaciones de RANITIDINA 150 mg de PHARMARKETING corresponden a DEXTROSA AL 5% EN SOLUCION SALINA ( SUERO MIXTO) M-007498-R1 Vencido 1999/01/01 IMPORTAR Y VENDER DELMED S.A. DE C.V.
Pasamos todas las presentaciones al Registro INVIMA 2005M-0004820
- El Registro M-007497 reportado para 6 de 8 presentaciones de RANITIDINA 300 mg de PHARMARKETING corresponden a DEXTROSA AL 33% EN AGUA DESTILADA INVIMA M-007497-R1 Vigente 2007/05/06 FABRICAR Y VENDER LABORATORIOS JUNIN LTDA. Aplicamos el Registro INVIMA 2005M-0004554 a todas las presentaciones.
- La búsqueda - 10796 - del Registro M-010796 reportado para SULFATO FERROSO 200 mg no produjo ningún resultado en la base de datos del INVIMA (5 presentaciones).
- La búsqueda - 07381 - del Registro M-007381 reportado para TRIMETOPRIM SULFAMETOXAZOL no produjo ningún resultado en la base de datos del INVIMA (5 presentaciones).
- PROCAPS
- El Registro M-001508 reportado para ALBENDAZOL 100 mg / 5 mL corresponde a ALANEX(R) JARABE INVIMA 2005M- 001508 - R1 de PRODUCTORA DE CAPSULAS DE GELATINA S.A., PROCAPS S.A.
Reporta VARCOR 80 mg en dos presentaciones con composición
de VARCOR H 80 mg + 12,5 mg
- REMO
- La búsqueda del registro M-003274 reportado para RANITIDINA 150 mg de REMO produce 4 resultados que no son de RANITIDINA en la base de datos del INVIMA. Solo aparece RANITIDINA TABLETAS X 300 MG INVIMA M-004215 Vencido 2006/02/19 FABRICAR Y VENDER LABORATORIO REMO LTDA
- SCANDINAVIA_PHARMA
El Registro M-014497 reportado para ABRILAR de SCANDINAVIA_PHARMA dá los siguientes resultados:
- IMPROSTAN 250MG M-014497 Vencido 2005/01/11 FABRICAR Y VENDER PATMAR S.A.
- UNIPRIL 5 MG TABLETAS. INVIMA M-014497 Vigente 2010/07/07 FABRICAR Y VENDER GRUPO FARMA DE COLOMBIA S.A.
Las búsquedas por ABRILAR, HEDERA, HELIX, por Nombre y Principio activo NO PRODUCEN NINGUN RESULTADO en la base de datos del INVIMA
- SERMA
- El Registro M-005968 reportado para RANITIDINA 300 mg de SERMA está errado. El correcto es INVIMA M-005986 y está vencido
- TRIDEX
- El Registro M-006005 reportado para ACETAMINOFEN 150 mg / 5 mL de TRIDEX corresponde a DIXICOL 150 mg / 5 mL de TRIDEX
- El Registro sanitario M-011870 reportado para FLUBENDAZOL 100 mg / 5 mL corresponde a
HELMIN EX 100 mg / 5 mL de GALEZ
- El Registro sanitario M-002995 reportado para SECNIDAZOL 500 mg corresponde a SEDAL 500 mg de GALEZ
- El Registro sanitario M-004285-R1 reportado para SULFATO FERROSO 180 mg corresponde a HEMOSINA 180 mg de TRIDEX y está vencido.
- El Registro sanitario M-008613-R1 reportado para TRIMETOPRIM SULFAMETOXAZOL
160 / 800 mg corresponde a MEDIPRIM F 160 / 800 mg de TRIDEX
- El Registro sanitario M- 008637 R-1 reportado para TRIMETOPRIM SULFAMETOXAZOL
40-200 mg / 5 mL corresponde a MEDIPRIM 40-200 mg/5 mL de TRIDEX
- VEFARCOL
- El Registro M-001907 reportado para RANITIDINA 50 mg / 2 mL de VEFARCOL está errado. La única RANITIDINA 50 mg / 2 mL de VEFARCOL en la base de datos del INVIMA tiene Registro INVIMA M-012132
- La búsqueda - 11496 - del Registro M-011496 reportado para TRIMETOPRIM SULFAMETOXAZOL coresponde a DICLOFENACO 50 MG TABLETAS INVIMA M-011496 de VEFARCOL S. A.
- VITALIS
- El Registro INVIMA M -011494 de N-BUTIL BROMURO DE HIOSCINA 20 mg / mL
de VITALIS es reportado además por BUSSIE y MEMPHIS
_________________________________________________________________________________________________
NOTA: Esta página funciona como memoria RAM. La lista es
parcial. Inclusiones y exclusiones a 27dic08 |
Actualizado por
Oscar Andia Salazar, MD
Vicepresidente de Política Farmacéutica Nacional
Federación Médica Colombiana / 27dic08
Favor enviar sus comentarios a andia@observamed.org
/ correo@medicentro.com.co
Visítenos en www.observamed.org
/ www.med-informatica.com
/ www.med-informatica.net
|

